Elagolix 834153-87-6
Dieses Medikament wird von Frauen zur Linderung mäßiger bis starker Schmerzen aufgrund einer Erkrankung namens Endometriose eingesetzt.
Kann behandeln: Endometriose
Markennamen: Orilissa
Wirkstoffklasse: LHRH (GnRH)-Antagonisten
Verfügbarkeit: Rezept erforderlich
Schwangerschaft: Vermeiden Sie die Anwendung während der Schwangerschaft
Stillzeit: Vor der Anwendung einen Arzt konsultieren
Elagolix ist eine oral bioverfügbare, nicht auf Peptiden basierende, niedermolekulare Verbindung der zweiten Generation und ein selektiver Gonadotropin-Releasing-Hormon (GnRH; LHRH)-Rezeptorantagonist mit potenziell hemmender Wirkung auf die Hormonproduktion. Bei oraler Verabreichung konkurriert Elagolix mit GnRH um die Rezeptorbindung und hemmt die Signalübertragung des GnRH-Rezeptors im Hypophysenvorderlappen. Dadurch wird die Ausschüttung des luteinisierenden Hormons (LH) und des follikelstimulierenden Hormons (FSH) gehemmt. Bei Männern verhindert die Hemmung der LH-Sekretion die Freisetzung von Testosteron. Bei Frauen verhindert die Hemmung von FSH und LH die Produktion von Östrogen in den Eierstöcken. Die Hemmung der GnRH-Signalübertragung kann Symptome von sexualhormonabhängigen Krankheitszuständen behandeln oder verhindern.
Elagolix ist ein oraler, nichtsteroidaler Antagonist des Gonadotropin-Releasing-Hormons (GnRH), der die Östrogenproduktion verringert und zur Behandlung schmerzhafter Formen der Endometriose bei Frauen eingesetzt wird. Die Elagolix-Therapie ist mit einer geringen Rate an Serumenzymerhöhungen während der Therapie verbunden und wurde bisher nicht mit Fällen klinisch erkennbarer Leberschäden in Verbindung gebracht.
Elagolix wurde in Studien zur Grundlagenforschung und Behandlung von Endometriose, Follikulogenese, Uterusmyomen, starken Uterusblutungen und starken Menstruationsblutungen eingesetzt. Am 24. Juli 2018 hat die US-amerikanische Food and Drug Administration (FDA) jedoch Elagolix von AbbVie unter dem Markennamen Orilissa als ersten und einzigen oralen Gonadotropin-Releasing-Hormon (GnRH)-Antagonisten zugelassen, der speziell für Frauen mit mittelschweren bis starken Endometriose-Schmerzen entwickelt wurde. Es wurde festgestellt, dass Endometriose eine der häufigsten gynäkologischen Erkrankungen in den Vereinigten Staaten ist. Schätzungen zufolge ist insbesondere jede zehnte Frau im gebärfähigen Alter von Endometriose betroffen und leidet unter schwächenden Schmerzsymptomen. Darüber hinaus können Frauen, die von dieser Erkrankung betroffen sind, bis zu sechs bis zehn Jahre lang leiden und mehrere Ärzte aufsuchen, bevor sie eine richtige Diagnose erhalten. Nachdem Orilissa (Elagolix) anschließend von der FDA im Rahmen einer vorrangigen Prüfung zugelassen wurde, bietet diese beschleunigte Neuzulassung medizinischem Fachpersonal eine weitere wertvolle Option zur Behandlung der potenziell ungedeckten Bedürfnisse von Frauen, die von Endometriose betroffen sind, abhängig von ihrer spezifischen Art und Schwere der Endometriose-Schmerzen .
Chemische Struktur
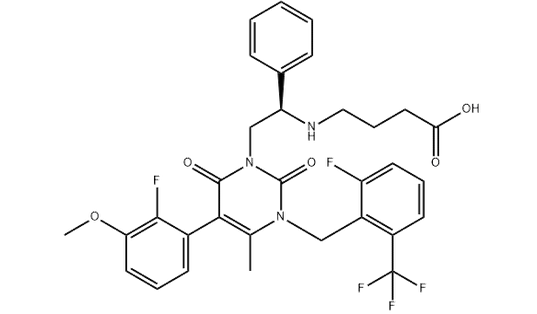





Vorschlag18Projekte zur Qualitätskonsistenzbewertung, die genehmigt wurden4, Und6Projekte befinden sich in der Genehmigungsphase.

Ein fortschrittliches internationales Qualitätsmanagementsystem hat eine solide Grundlage für den Vertrieb gelegt.

Die Qualitätsüberwachung erstreckt sich über den gesamten Lebenszyklus des Produkts, um die Qualität und therapeutische Wirkung sicherzustellen.

Ein professionelles Regulatory-Affairs-Team unterstützt die Qualitätsansprüche bei der Antragstellung und Registrierung.


Korea Countec Flaschenverpackungslinie


Taiwan CVC-Flaschenverpackungslinie


Italien CAM Kartonverpackungslinie

Deutsche Fette-Verdichtungsmaschine

Japan Viswill Tablet-Detektor

DCS-Kontrollraum







