Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) ist eine Hauptart der Herzinsuffizienz, und die China HF Study zeigte, dass 42 % der Herzinsuffizienz in China HFrEF sind, obwohl mehrere Standardtherapieklassen von Medikamenten für HFrEF verfügbar sind und das Risiko verringert haben Todesfälle und Krankenhausaufenthalte wegen Herzinsuffizienz bis zu einem gewissen Grad. Bei Patienten besteht jedoch ein hohes Risiko für eine wiederkehrende Verschlechterung der Herzinsuffizienz, die Sterblichkeit liegt weiterhin bei etwa 25 % und die Prognose ist nach wie vor schlecht. Daher besteht nach wie vor ein dringender Bedarf an neuen Therapeutika für die Behandlung von HFrEF, und Vericiguat, ein neuartiger Stimulator der löslichen Guanylatzyklase (sGC), wurde in der VICTORIA-Studie untersucht, um zu beurteilen, ob Vericiguat die Prognose von Patienten mit HFrEF verbessern könnte. Bei der Studie handelt es sich um eine multizentrische, randomisierte, placebokontrollierte, doppelblinde, ereignisgesteuerte Phase-III-Ergebnisstudie mit Parallelgruppen. An der Studie, die unter der Schirmherrschaft des VIGOR Centre in Kanada in Zusammenarbeit mit dem Duke Clinical Research Institute durchgeführt wurde, beteiligten sich 616 Zentren in 42 Ländern und Regionen, darunter Europa, Japan, China und den Vereinigten Staaten. Unsere kardiologische Abteilung hatte die Ehre, teilnehmen zu dürfen. Insgesamt 5.050 Patienten mit chronischer Herzinsuffizienz im Alter von ≥ 18 Jahren, NYHA-Klasse II-IV, EF <45 %, mit erhöhten natriuretischen Peptid (NT-proBNP)-Spiegeln innerhalb von 30 Tagen vor der Randomisierung und die wegen Herzinsuffizienz ins Krankenhaus eingeliefert wurden innerhalb von 6 Monaten vor der Randomisierung oder denen innerhalb von 3 Monaten vor der Randomisierung Diuretika gegen Herzinsuffizienz intravenös verabreicht wurden, wurden in die Studie aufgenommen, alle erhielten ESC, AHA/ACC und Nationale/regionale Richtlinien, empfohlener Pflegestandard. Die Patienten wurden im Verhältnis 1:1 in zwei Gruppen randomisiert und erhaltenVericiguat(n=2526) bzw. Placebo (n=2524) zusätzlich zur Standardtherapie.
Der primäre Endpunkt der Studie war der kombinierte Endpunkt aus kardiovaskulärem Tod oder erster Krankenhauseinweisung aufgrund von Herzversagen; Zu den sekundären Endpunkten gehörten Komponenten des primären Endpunkts, erste und nachfolgende Krankenhauseinweisungen wegen Herzinsuffizienz (erstes und wiederkehrendes Ereignis), der zusammengesetzte Endpunkt aus Gesamttod oder Krankenhauseinweisung wegen Herzinsuffizienz und Gesamttod. Bei einer mittleren Nachbeobachtungszeit von 10,8 Monaten kam es in der Vericiguat-Gruppe im Vergleich zur Placebo-Gruppe zu einer relativen Reduzierung des primären Endpunkts kardiovaskulärer Tod oder erster Krankenhausaufenthalt wegen Herzinsuffizienz um 10 %.
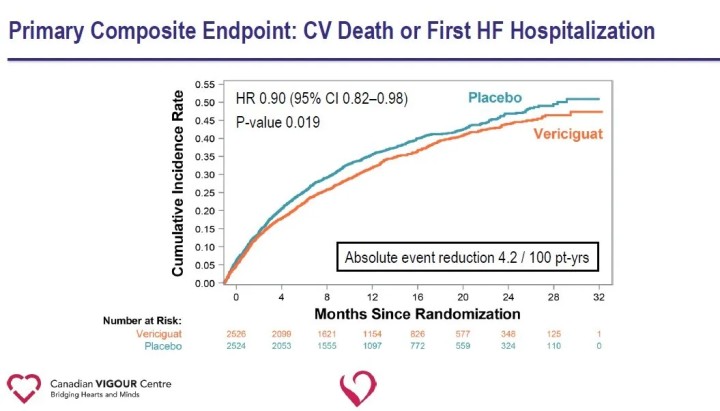
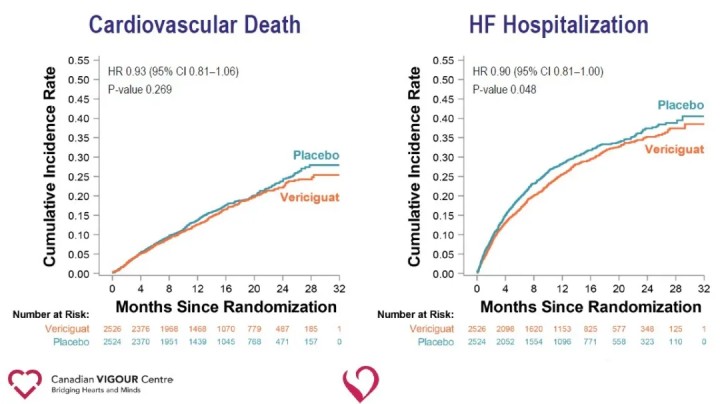
Die Analyse sekundärer Endpunkte zeigte eine signifikante Verringerung der Krankenhauseinweisungen wegen Herzinsuffizienz (HR 0,90) und eine signifikante Verringerung des kombinierten Endpunkts Gesamttod oder Krankenhauseinweisungen wegen Herzinsuffizienz (HR 0,90) in der Vericiguat-Gruppe im Vergleich zur Placebogruppe.
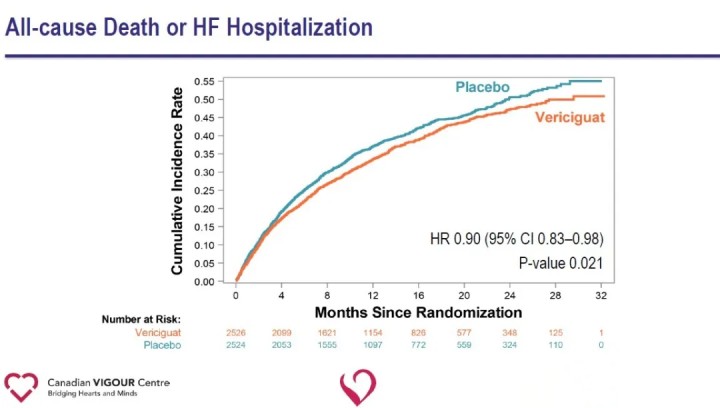
Die Ergebnisse der Studie legen nahe, dass der Zusatz vonVericiguatIm Vergleich zur Standardbehandlung der Herzinsuffizienz verringert sich das kürzlich aufgetretene Auftreten sich verschlechternder Herzinsuffizienzereignisse erheblich und das Risiko des kombinierten Endpunkts kardiovaskulärer Tod oder Krankenhausaufenthalt wegen Herzinsuffizienz bei Patienten mit HFrEF. Die Fähigkeit von Vericiguat, das Risiko des kombinierten Endpunkts kardiovaskulärer Tod oder Krankenhausaufenthalt aufgrund von Herzinsuffizienz bei Patienten mit Hochrisiko-Herzinsuffizienz zu reduzieren, bietet einen neuen therapeutischen Weg für Herzinsuffizienz und eröffnet neue Wege für die zukünftige Erforschung von Herz-Kreislauf-Erkrankungen. Vericiguat ist derzeit nicht für die Vermarktung zugelassen. Die Sicherheit, Wirksamkeit und Kosteneffizienz des Arzneimittels müssen noch weiter auf dem Markt getestet werden.
Zeitpunkt der Veröffentlichung: 09.02.2022
